Qu’est-ce que la Recherche Clinique ?
La recherche clinique comprend l’ensemble des essais cliniques menés sur la personne humaine (saine ou malade) dans le but d’améliorer les connaissances biologiques et médicales des maladies. Elle est indispensable à la mise au point de nouveaux traitements, dispositifs médicaux ou de nouvelles méthodes de diagnostic afin d’améliorer la prise en charge thérapeutique des patients. Elle est cadrée par une méthodologie et une législation rigoureuse.
En France, la recherche clinique est régie par :
- La Loi Jardé n° 2012- 300 du 05 mars 2012 modifiée par Ordonnance n° 2016-800, décret d’application 2016-1537 du 16 Novembre 2016 relative aux recherches impliquant la personne humaine.
- Le Règlement européen sur la protection des données et le traitement des données de santé ainsi que les droits des personnes
- Les bonnes pratiques cliniques (BPC) définies par l'ensemble des dispositions à mettre en place pour assurer, à des essais, la qualité et l'authenticité de leurs données scientifiques d'une part, et le respect de l'éthique d'autre part.
Ainsi, le Recherche Clinique permet de:
- tester de nouveaux médicaments ou de nouveaux dispositifs médicaux en vue de leur autorisation de mise sur le marché ou d’une extension des indications thérapeutiques pour des médicaments déjà existant
- comparer des stratégies thérapeutiques ou des techniques de diagnostic innovantes à celles déjà existantes
Pour en savoir plus sur les différentes étapes de développement d’un médicament ou d’un dispositif médical, vous pouvez cliquer ci-dessous :
- Les différentes étapes dans le développement d’un médicament
- Les différentes étapes dans le développement d’un dispositif médical
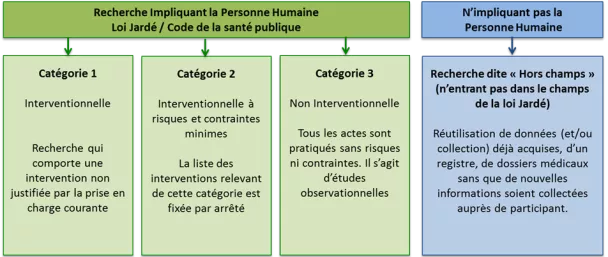
Selon la Loi Jardé, il existe 3 grandes catégories de recherche impliquant la personne humaine (RIPH) (Catégorie 1 et 2 et 3) :